IDENTIFICA LA FORMULAS DE LOS SIGUIENTES COMPUESTOS.
1.- ANHIDRIDO SULFURICO SO( ) SO3( X )
2.- MONOXIDO DE CARBONO CO( ) CO( X )
3.- ÓXIDO DE CLORO(i) CL2O( X ) Cl( )
4.-MONOXIDO DE DIBROMO BrO( ) Br2O( X )
5.- DIOXIDO DE SICILIO SlO3( ) SiO2( X )
martes, 30 de octubre de 2012
HIDRÓXIDOS AL COMBINARSE CON LOS CATIONES
CATIÓN OH- GINEBRA UIQPA
-Li+ -LiOH -Hidroxido de litio -Hidroxido de litio
-Fe3+ -Fe(OH)3 -Hidroxido ferrico -Hidroxido de fierro (III)
-Ba2+ -Ba(OH)2 -Hidroxido de bario -Hidroxido de bario(II)
-Co3+ -Co(OH)3 -Hidroxido cobaltico -Hidroxido de cobalto(III)
-Mg2+ -Mg(OH)2 -Hidroxido de magnesio -Hidroxido de magnesio(II)
CATIÓN OH- GINEBRA UIQPA
-Li+ -LiOH -Hidroxido de litio -Hidroxido de litio
-Fe3+ -Fe(OH)3 -Hidroxido ferrico -Hidroxido de fierro (III)
-Ba2+ -Ba(OH)2 -Hidroxido de bario -Hidroxido de bario(II)
-Co3+ -Co(OH)3 -Hidroxido cobaltico -Hidroxido de cobalto(III)
-Mg2+ -Mg(OH)2 -Hidroxido de magnesio -Hidroxido de magnesio(II)
ORIGEN DEL NOMBRE DE ALGUNOS ELEMENTOS
ELEMENTO SIMBOLO ORIGEN DEL NOMBRE
-Curio -Cm -En honor de pierre y marie curie.
-Einstenio -Es -En honor a Albert Einstein.
-Californio -Cf -Descubierto en California.
-Rutenio -Ru -Del latin ruteria, que significa Rusia.
-Titanio -Ti -Derivado de los titanes, personajes
mitológicos griegos.
-Circonio -Zr -Del arabe zargún, color dorado.
-Uranio -U -Por el planeta Urano.
ELEMENTO SIMBOLO ORIGEN DEL NOMBRE
-Curio -Cm -En honor de pierre y marie curie.
-Einstenio -Es -En honor a Albert Einstein.
-Californio -Cf -Descubierto en California.
-Rutenio -Ru -Del latin ruteria, que significa Rusia.
-Titanio -Ti -Derivado de los titanes, personajes
mitológicos griegos.
-Circonio -Zr -Del arabe zargún, color dorado.
-Uranio -U -Por el planeta Urano.
Compuestos binarios
Estos compuestos químicos formado por átomos de sólo dos elementos. Se distinguen dos grupos principales de compuestos binarios.
° Compuestos iónicos binarios: donde se incluyen las sales binarias, óxidos metálicos y los hidruros metálicos.
Estos compuestos químicos formado por átomos de sólo dos elementos. Se distinguen dos grupos principales de compuestos binarios.
° Compuestos iónicos binarios: donde se incluyen las sales binarias, óxidos metálicos y los hidruros metálicos.
Compuestos covalentes binarios: donde se incluyen los óxidos no metálicos y los halógenos de no metálicos..jpg)
.jpg)
lunes, 29 de octubre de 2012
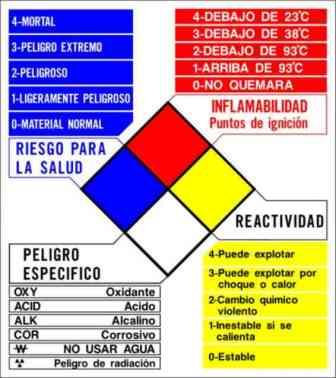
PICTOGRAMAS DE SEGURIDAD
| |||||||||||||||||||||||||||||||||||||||||||||||||||
HIDRUROS METÁLICOS
Ión metálico H- Ginebra UIQPA
-k+ -KH -Hidruro de potasio -Hidruro de potasio
-Mg2+ -MgH2 -Hidruro de magnesio -Hidruro de mangnesio
-Fe3+ -FeH3 -Hidruro ferrico -Hidruro de hierro(III)
-Co3+ -CoH3 -Hidruro cobaltico -Hidruro de cobalto(III)
-Ni3+ -NiH3 -Hidruro niquelico -Hidruro de niquel(III)
Ión metálico H- Ginebra UIQPA
-k+ -KH -Hidruro de potasio -Hidruro de potasio
-Mg2+ -MgH2 -Hidruro de magnesio -Hidruro de mangnesio
-Fe3+ -FeH3 -Hidruro ferrico -Hidruro de hierro(III)
-Co3+ -CoH3 -Hidruro cobaltico -Hidruro de cobalto(III)
-Ni3+ -NiH3 -Hidruro niquelico -Hidruro de niquel(III)
NOMENCLATURA DE LOS COMPUESTOS CUATERNARIOS.
Ejemplos de sales oxidas
Ca(HSO2)2-------------------------- hidrogeno hiposulfuroso de calcio
Pb(HSO3)4-------------------------- hidrogeno sulfito de plomo (iv)
Cr(HSO4)3--------------------------hidrogeno sulfato de cromo (iii)
Sr(H3As2O5)2----------------------trihidrogeno piroarseniato de estroncio.
Mg(H2Sb2O5)----------------------dihidrogeno piroantimonio de magnesio.
Ejemplos de sales oxidas
Ca(HSO2)2-------------------------- hidrogeno hiposulfuroso de calcio
Pb(HSO3)4-------------------------- hidrogeno sulfito de plomo (iv)
Cr(HSO4)3--------------------------hidrogeno sulfato de cromo (iii)
Sr(H3As2O5)2----------------------trihidrogeno piroarseniato de estroncio.
Mg(H2Sb2O5)----------------------dihidrogeno piroantimonio de magnesio.
sábado, 27 de octubre de 2012
jueves, 25 de octubre de 2012
PRACTICA.- MEZCLAS Y MODOS DE SEPARACIÓN
MATERIAL
MEZCLA SOLUBLE/INSOLUBLE CLASIFICACIÓN MÉTODO DE S. USADO
Agua+NaCl -soluble -homogenéa -evaporación -mechero, manguera de latex, vaso de precipitado.
Agua+S -insoluble -heterogenea -filtración -papel filtro, embudo
Agua+
limadura de -insoluble -heterogenea -imantación -vaso de precipitado,
Fe. un imán
Agua+
aceite -insoluble -heterogenea -decantación -embudo de
separación, vaso de
precipitado.
Agua+
alcohol. -insoluble -heterogenea -destilación -soporte universal,
matraz de destilación,
termometro, tubo de
refrigeración, regilla,
mechero bunsen.
jueves, 18 de octubre de 2012
PRACTICA
IDENTIFICACIÓN DE ÁCIDOS Y BASESEl grupo 11b6 en la clase de química-laboratorio, realizamos un interesante pero un poco peligroso experimento ''La identificación de un ácido y una base''.
¿Porqué peligroso experimento? esto se debió a los fuertes gases que el azufre libero al calentarlo y ponerlo después sobre el agua.
Después había que identificar la base es decir la cinta de magnesio en contacto con el fuego.
ÁCIDOS Y BASES
En esta practica veremos las diferencias que hay entre una base y un ácido pero primero identificaremos que sustancia resulta ser el ácido y cual la base.Para ello necesitaremos de muchos y diversos materiales, a si como de algunas sustancias químicas en este caso azufre y cinta de magnesio conocimientos previos sobre que es un ácido y una base, a si como todas sus características.
El objetivo de esta practica es averiguar que sustancia resulta ser un ácido y cual una base.
MATERIALES
Mechero bunsen.Manguera de látex.
Cerillos ó un encendedor.
Matraz erlenmeyer.
100 mililitros de agua.
Cucharilla de metal.
Papel tornasol.
2 hojas de papel.
Un vidrio de reloj.
Pinzas.
SUSTANCIAS
Las sustancias que usaremos son lo mínimo posible de azufre, esto para evitar crear demasiados vapores olorosos, y un pequeño trozo de cinta de magnesio.OBSERVACIONES
Una vez que calentamos el azufre y lo metimos en el matraz, empezó a soltar vapores muy fuertes, que irritan la nariz e incluso te arden los ojos.CONCLUSIONES
Los fuertes vapores nos dio a conocer que el azufre era el azufre era el ácido y la base fue la cinta de magnesio.


viernes, 12 de octubre de 2012
COMPUESTO NOMBRE FLAMA
-MgCl2 -Bicloruro de magnesio -Flama amarilla y mucho humo.
-CuSO4 -sulfato de cobre -Flama verde y bastante humo.
-SrCl2 -Cloruro de estroncio -Flama roja con humo.
-LiCl -Cloruro de litio -Flama roja, acompañado de chispas.
-KCl -Cloruro de potasio -Flama naranja durazno.
-NaCl -Cloruro de sodio -Flama naranja vivo y acompañado de
muchas chispas
-MgCl2 -Bicloruro de magnesio -Flama amarilla y mucho humo.
-CuSO4 -sulfato de cobre -Flama verde y bastante humo.
-SrCl2 -Cloruro de estroncio -Flama roja con humo.
-LiCl -Cloruro de litio -Flama roja, acompañado de chispas.
-KCl -Cloruro de potasio -Flama naranja durazno.
-NaCl -Cloruro de sodio -Flama naranja vivo y acompañado de
muchas chispas
jueves, 11 de octubre de 2012
Configuraciones electrónicas del Hidrógeno (1) al Indio (49)
Hidrógeno H (1)= 1s1
Helio He (2)= 1s2
Litio Li (3)= 1s2 2s1
Berilio (Be) 4= 1s2 2s2
Boro (B) 5 = 1s2 2s2 2p1
Carbono (C) 6= 1s2 2s2 2p2
Nitrógeno (N )7= 1s2 2s2 2p3
Oxígeno (O) 8= 1s2 2s2 2p4
Flúor (F) 9= 1s2 2s2 2p5
Neón (Ne) 10= 1s2 2s2 2p6
Sodio (Na) 11= 1s2 2s2 2p6 3s1
Magnesio (Mg) 12= 1s2 2s2 2p6 3s2
Aluminio (Al) 13= 1s2 2s2 2p6 3s2 3p1
Silicio (Si) 14= 1s2 2s2 2p6 3s2 3p2
Fósforo (P) 15= 1s2 2s2 2p6 3s2 3p3
Azufre (S) 16= 1s2 2s2 2p6 3s2 3p4
Cloro (Cl) 17= 1s2 2s2 2p6 3s2 3p5
Argón (Ar) 18 = 1s2 2s2 2p6 3s2 3p6
Potasio (K) 19= 1s2 2s2 2p6 3s2 3p6 4s1
Calcio (Ca) 20= 1s2 2s2 2p6 3s2 3p6 4s2
Escandio (Sc) 21= 1s2 2s2 2p6 3s2 3p6 4s2 3d1
Titanio (Ti) 22= 1s2 2s2 2p6 3s2 3p6 4s2 3d2
Vanadio (V) 23= 1s2 2s2 2p6 3s2 3p6 4s2 3d3
Cromo (Cr) 24= 1s2 2s2 2p6 3s2 3p6 4s2 3d4
Manganeso (Mn) 25= 1s2 2s2 2p6 3s2 3p6 4s2 3d5
Fierro (Fe) 26= 1s2 2s2 2p6 3s2 3p6 4s2 3d6
Cobalto (Co) 27= 1s2 2s2 2p6 3s2 3p6 4s2 3d7
Níquel (Ni) 28= 1s2 2s2 2p6 3s2 3p6 4s2 3d8
Cobre (Cu) 29= 1s2 2s2 2p6 3s2 3p6 4s2 3d9
Zinc (Zn) 30= 1s2 2s2 2p6 3s2 3p6 4s2 3d10
Galio (Ga) 31= 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p1
Germanio (Ge) 32= 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p2
Arsénico (As) 33= 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p3
Selenio (Se) 34= 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p4
Bromo (Br) 35= 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p5
Criptón (K) 36= 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6
Rubidio (Rb) 37 = 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s1
Estroncio (Sr) 38= 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2
Itrio (Y) 39= 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d1
Circonio (Zr) 40= 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d2
Niobio (Nb) 41= 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d3
Molibdeno (Mo) 42= 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d4
Tecnecio (Tc) 43= 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d5
Rutenio (Ru) 44= 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d6
Rodio (Rh) 45= 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d7
Paladio (Pd) 46= 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d8
Plata (Ag) 47= 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d9
Cadmio (Cd) 48= 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10
Indio (In) 49= 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p1
Hidrógeno H (1)= 1s1
Helio He (2)= 1s2
Litio Li (3)= 1s2 2s1
Berilio (Be) 4= 1s2 2s2
Boro (B) 5 = 1s2 2s2 2p1
Carbono (C) 6= 1s2 2s2 2p2
Nitrógeno (N )7= 1s2 2s2 2p3
Oxígeno (O) 8= 1s2 2s2 2p4
Flúor (F) 9= 1s2 2s2 2p5
Neón (Ne) 10= 1s2 2s2 2p6
Sodio (Na) 11= 1s2 2s2 2p6 3s1
Magnesio (Mg) 12= 1s2 2s2 2p6 3s2
Aluminio (Al) 13= 1s2 2s2 2p6 3s2 3p1
Silicio (Si) 14= 1s2 2s2 2p6 3s2 3p2
Fósforo (P) 15= 1s2 2s2 2p6 3s2 3p3
Azufre (S) 16= 1s2 2s2 2p6 3s2 3p4
Cloro (Cl) 17= 1s2 2s2 2p6 3s2 3p5
Argón (Ar) 18 = 1s2 2s2 2p6 3s2 3p6
Potasio (K) 19= 1s2 2s2 2p6 3s2 3p6 4s1
Calcio (Ca) 20= 1s2 2s2 2p6 3s2 3p6 4s2
Escandio (Sc) 21= 1s2 2s2 2p6 3s2 3p6 4s2 3d1
Titanio (Ti) 22= 1s2 2s2 2p6 3s2 3p6 4s2 3d2
Vanadio (V) 23= 1s2 2s2 2p6 3s2 3p6 4s2 3d3
Cromo (Cr) 24= 1s2 2s2 2p6 3s2 3p6 4s2 3d4
Manganeso (Mn) 25= 1s2 2s2 2p6 3s2 3p6 4s2 3d5
Fierro (Fe) 26= 1s2 2s2 2p6 3s2 3p6 4s2 3d6
Cobalto (Co) 27= 1s2 2s2 2p6 3s2 3p6 4s2 3d7
Níquel (Ni) 28= 1s2 2s2 2p6 3s2 3p6 4s2 3d8
Cobre (Cu) 29= 1s2 2s2 2p6 3s2 3p6 4s2 3d9
Zinc (Zn) 30= 1s2 2s2 2p6 3s2 3p6 4s2 3d10
Galio (Ga) 31= 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p1
Germanio (Ge) 32= 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p2
Arsénico (As) 33= 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p3
Selenio (Se) 34= 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p4
Bromo (Br) 35= 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p5
Criptón (K) 36= 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6
Rubidio (Rb) 37 = 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s1
Estroncio (Sr) 38= 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2
Itrio (Y) 39= 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d1
Circonio (Zr) 40= 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d2
Niobio (Nb) 41= 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d3
Molibdeno (Mo) 42= 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d4
Tecnecio (Tc) 43= 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d5
Rutenio (Ru) 44= 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d6
Rodio (Rh) 45= 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d7
Paladio (Pd) 46= 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d8
Plata (Ag) 47= 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d9
Cadmio (Cd) 48= 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10
Indio (In) 49= 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p1
miércoles, 10 de octubre de 2012
Suscribirse a:
Entradas (Atom)
.jpg)
.jpg)
.jpg)
.jpg)
.jpg)